Ao estudarmos o comportamento dos gases, algumas variáveis devem ser consideradas. As variáveis de estado de um gás são: volume, pressão e temperatura.
Vejamos cada uma delas:
• Volume dos gases (V):
Em qualquer situação, o volume do gás é igual ao volume do recipiente que o contém.
No Sistema Internacional (SI), a unidade do volume é o metro cúbico (m3). Mas outras unidades são muito utilizadas usualmente, como o litro (L), mililitros (mL), centímetros cúbicos (cm3), densímetros cúbicos (dm3), entre outros. Algumas relações entre essas unidades são dadas abaixo:

• Pressão dos gases (P):

Matematicamente, podemos calcular essa pressão pela equação: P = F/S. Ou seja, é o mesmo que distribuir a força em cada unidade de área.
Essa pressão é resultado das colisões existentes entre as moléculas do gás e as paredes do recipiente que as contém. Assim, quanto maior a quantidade de partículas por área, maior será a pressão exercida.

Os gases atmosféricos causam uma pressão sobre a superfície terrestre, que é denominada pressão atmosférica.
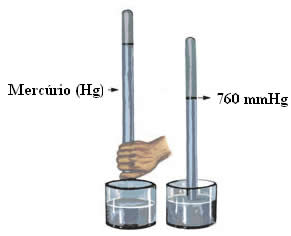
A pressão atmosférica foi medida pela primeira vez em 1643, pelo físico e matemático italiano Evangelista Torricelli (1608-1647). Ele fez isto a partir do tubo de Torricelli (barômetro de mercúrio), que funcionou da seguinte maneira: em um recipiente contendo mercúrio (Hg), Torricelli virou um tubo de vidro contendo também mercúrio. Ele percebeu que, ao nível do mar, o líquido não escoava completamente e que havia um espaço vazio no interior da coluna (vácuo). A altura que o mercúrio descia era de 760 mm. Esta era proporcional à pressão exercida pelo ar. Desse modo, o valor universal para a pressão atmosférica é de 760mm Hg.
A unidade no SI é o Pascal (Pa = N/m2), no entanto, de maneira usual, o bar também é aceito. Outras unidades, como o atm e o torr, não são recomendadas. Veja a relação dessas unidades:
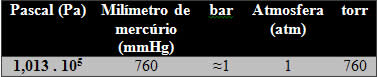
Um fator importante é que à medida que a altitude aumenta, a pressão diminui, por isso esses valores citados são dados para o nível do mar.
• Temperatura dos gases (P):
A temperatura mede o grau de agitação das partículas (átomos ou moléculas) do gás. Quanto maior o grau de agitação dessas partículas, maior será sua temperatura e a sua pressão.
Normalmente, os valores da temperatura são dados por um termômetro, cuja graduação termométrica ou escala termométrica no SI é o Kelvin (K), que é chamada de escala absoluta. Outras unidades usuais são a escala Celsius (°C) e a escala Fahrenheit (°F).
0°C equivale a 273 K, e 373K corresponde a 100°C. Isto significa que para se converter o grau Celsius em Kelvin, basta somar 273: TK = T°C + 273.