Daí o significado do nome “isotérmico”, que vem do grego, em que iso significa “igual” ethermo é “calor”, ou seja, “calor igual” ou “temperatura igual, constante”.
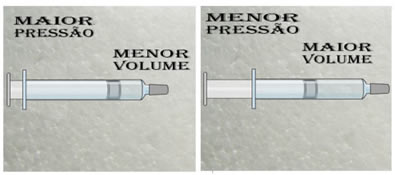
Para ver como o volume varia em relação à pressão, imagine uma seringa, cujo orifício está fechado e o êmbolo pressionado. Veremos que quanto maior for a pressão externa aplicada sobre o êmbolo da seringa, menor será o volume do ar dentro da seringa.
Essa relação entre o volume e a pressão, com a temperatura de uma massa de gás fixa, foi estudada pela primeira vez pelo físico e naturalista inglês Robert Boyle (1627-1691), que realizou experimentos isotérmicos bem controlados, comprovando que o volume é inversamente proporcional à pressão.
Quatorze anos depois, o físico francês Edme Mariotte (1620-1684) realizou os mesmos experimentos e os divulgou na França, honestamente lembrando-se de Boyle. Assim, criou-se a seguinte lei sobre transformações isotérmicas com gases, denominada Lei de Boyle-Mariotte:

Isso significa que, por exemplo, se diminuirmos o volume pela metade, a pressão exercida pelas moléculas do gás dobrará e assim sucessivamente, como pode ser visto abaixo:
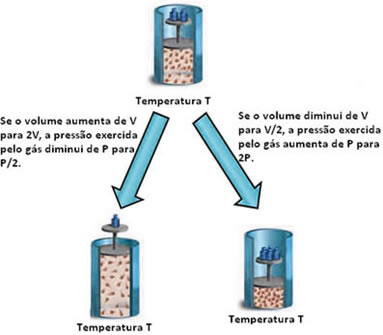
Matematicamente, temos:

k é a constante de proporcionalidade, ou seja, sempre que duas grandezas variam numa mesma proporção, a multiplicação entre elas dá uma constante. Assim, não importa se alteramos a pressão do sistema e, consequentemente, o volume; o produto dos dois sempre será o mesmo.
Portanto, podemos escrever:

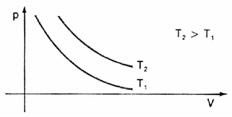
Representando graficamente essas variações do volume em relação à pressão, veremos que sempre dará uma curva denominada hipérbole, que chamamos, nesse caso, de isoterma. Diferentes temperaturas originam diferentes isotermas: