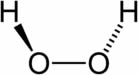Óxidos são compostos binários, ou seja, formados pela combinação de dois elementos, sendo um deles oxigênio.
Classificação dos óxidos em função do comportamento na presença de outros elementos:
Óxidos básicos: o metal presente em sua fórmula pode apresentar “carga elétrica” +1 e +2, ou seja, possuir caráter iônico. Exemplos: Na2O (Óxido de sódio), BaO (Óxido de bário). Em razão dessa propriedade, estes compostos reagem com ácidos e originam sal e água. Veja o processo:
Na2O + H2SO4 → Na2SO4 + H2O
óxido básico + ácido sal água
Óxidos neutros: são compostos por ametais, eles não reagem com água, ácido ou base, em razão da ligação covalente que une seus componentes, daí o porquê de serem chamados de óxidos inertes. Exemplos: monóxido de dinitrogênio (N2O), monóxido de carbono (CO).
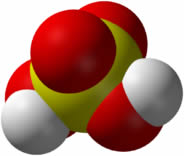
Óxidos ácidos: também conhecidos como anidridos de ácidos, são formados por ametais e apresentam caráter covalente. Na presença de água produzem ácidos e na presença de bases originam sal e água. Exemplo: CO2 (dióxido de carbono ou gás carbônico), SO2 (óxido de enxofre).
Óxidos duplos ou mistos: a combinação de dois óxidos de um mesmo elemento dá origem a esse tipo de óxido. Exemplo: magnetita (Fe3O4), junção dos óxidos Ferro (Fe) e Oxigênio (O). Aplicação: ímã natural.
Óxidos anfóteros: apresentam ambiguidade, na presença de um ácido se comportam como óxidos básicos, e na presença de uma base, como óxidos ácidos. Exemplos: óxido de Alumínio (Al2O3), óxido de zinco (ZnO).
Peróxidos: compostos que possuem em sua fórmula o grupo (O2)2- . Exemplos: Água oxigenada (H2O2) e Peróxido de sódio (Na2O2).
Os peróxidos mais comuns são formados por hidrogênio, metais alcalinos e metais alcalino-terrosos. São aplicados na indústria como alvejantes para clarificar tecidos e polpa de celulose (confecção de papel).
Aproveite para conferir nossas videoaulas relacionadas ao assunto: