As observações científicas, feitas por meio de experiências controladas e que levam ao desenvolvimento de teorias e leis, necessitam de medições específicas, principalmente para que, além de serem exatas, possam também ser repetidas quantas vezes for necessário e por qualquer pessoa no mundo. Essas medições podem ser feitas da massa, do volume, da temperatura etc. Tudo aquilo que pode ser medido é chamado de grandeza.
Cada grandeza é expressa em números e possui uma unidade padrão que é escolhida previamente para servir de comparação para outras medidas dessa mesma natureza. Por exemplo, a massa dos corpos é uma grandeza que pode ser medida em gramas, quilogramas, miligramas, toneladas e assim por diante. Mas a unidade padrão, que é a unidade internacional de massa, é o quilograma (kg). Assim, quando se diz que a massa de determinado corpo é 50 kg, isso significa que, em comparação com o padrão escolhido, que é o kg, a massa desse corpo é 50 vezes maior.
As demais unidades são múltiplos e submúltiplos, por exemplo, a tonelada é um múltiplo (1 tonelada = 1 000 kg) e o grama é um submúltiplo do quilograma (1 grama = 10-3 kg).
As unidades padrões são diferentes para cada tipo de grandeza e são estabelecidas pelo Sistema Internacional de Unidades (SI), e a IUPAC (União Internacional de Química Pura e Aplicada) os adota.
Veja a seguir quais são as unidades de medida mais importantes para um estudo inicial da Química:
- Massa (m): indica a quantidade de matéria que existe num corpo, sendo que sua medida é feita numa balança.

Conforme já mencionado, a unidade padrão de massa do SI é o quilograma (kg).
Observação: É importante ressaltar que massa é uma grandeza diferente de peso (P), sendo que este último é dado pela multiplicação da massa do corpo pela aceleração da gravidade local (P = m.g). Sua unidade é o Newton (1 N = 1 kg . m/s2). Todo corpo tem massa, mesmo que esteja isolado, mas o peso só terá aquele corpo que estiver próximo de outro corpo que o atraia. Por exemplo, o nosso peso, na verdade, não é o valor dado na balança; isso é a nossa massa. O peso é a força com que a Terra nos atrai para a sua superfície.
- Volume (V): é a extensão do espaço ocupado por um corpo.
Sua medida é feita por meio de recipientes apropriados, como os mostrados abaixo, que possuem graduações em suas paredes.
.jpg)
O volume é derivado das unidades de comprimento, sendo que para um cubo ele pode ser determinado pela fórmula:
Volume = comprimento . altura . largura
Visto que a unidade padrão de comprimento é o metro (m), a unidade de volume no SI é metro cúbico (m3). No entanto, outras unidades acabam sendo mais utilizadas no cotidiano, tais como o litro (L) e o mililitro (mL). Veja as correspondências abaixo:
1 m3 = 1000 L ou 1000 dm3
1 dm3 = 1 L
1 cm3 = 1 mL
1 cm3 ou 1 mL = 10-3 dm3 ou 10-3 L
- Temperatura (T): é a medida do nível de energia térmica de um material.
Sua medida é feita por meio de termômetros, um fino tubo graduado que contém mercúrio em seu interior. À medida que fica mais quente, o mercúrio se expande e mostra na graduação ao longo do tubo qual é a temperatura.

A unidade padrão no SI para a temperatura é o Kelvin (K), que é reconhecido como escala absoluta. Mas, no Brasil, costuma-se usar a escala Celsius (ºC). Para entender como realizar conversões entre essas escalas termométricas leia o texto abaixo:
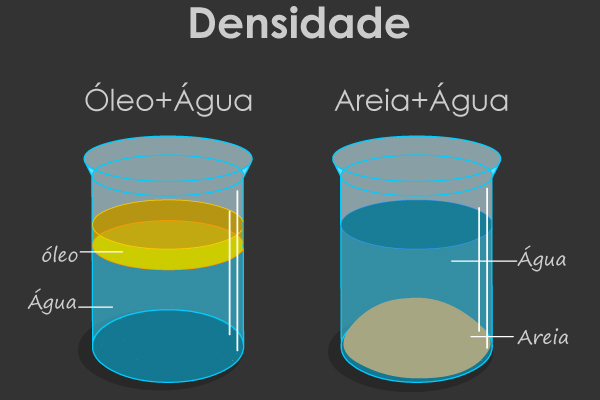
- Densidade (d) ou massa específica: é a relação entre a massa (m) e o volume (V) de um material.
d = m (g)
V (cm3 ou L)
O objeto que tiver maior densidade afunda em relação a outro com menor densidade e vice-versa. Por exemplo, os icebergs são gigantescos blocos de gelo, no entanto, eles flutuam sobre a água do mar. Isso ocorre porque como são apenas água pura solidificada, a sua densidade é de 0,92 g/cm3, enquanto a densidade da água do mar, que contém sais, é maior (1,03 g/cm3).

Para sólidos e líquidos, a unidade usada para a densidade costuma ser o gramas por centímetros cúbicos (g/cm3), já para gases, usa-se o gramas por litro (g/L).
Um aparelho usado para medir a densidade de líquidos e soluções é o densímetro, mostrado abaixo:
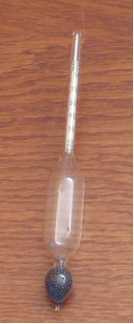
Mais detalhes sobre esse assunto se encontram no texto: Densidade.
- Pressão (p): é a força aplicada sobre um corpo dividida pela área sobre a qual a força (F) é exercida.
p = F
a
A unidade padrão de pressão no SI é o pascal (Pa), que é 1 Newton sobre 1 metro quadrado (1 Pa = 1 N/m2), mas outras unidades costumam ser utilizadas, tais como o milímetro de mercúrio (mmHg) e o atmosfera (atm).
A pressão atmosférica ao nível do mar é igual a 1 atm ou 760 mmHg, que correspondem a 1,01325 . 105 Pa. Essa pressão foi medida pela primeira vez por Torricelli. Veja seu experimento no texto: Como medir a pressão atmosférica?
A pressão diminui com o aumento da altitude e pode ser medida por meio de um equipamento chamado barômetro (imagem abaixo).
.jpg)
Videoaulas relacionadas: