No ano de 1884, o químico, físico e matemático sueco Svante August Arrhenius (1859-1927) realizou diversos experimentos na Universidade de Upsala, na Suécia, e, baseado nos resultados obtidos, propôs a Teoria da Dissociação Iônica, que lhe rendeu o Prêmio Nobel em 1903.
.jpg)
Arrhenius utilizou um equipamento parecido com o mostrado a seguir. Nele, temos uma bateria, em que de um de seus polos sai um eletrodo (fio de cobre) conectado a uma lâmpada e o outro fio fica com a extremidade solta. Ele colocava as duas extremidades dos eletrodos em contato com diferentes tipos de soluções e observava se havia passagem de corrente elétrica, o que era evidenciado quando a lâmpada acendia.
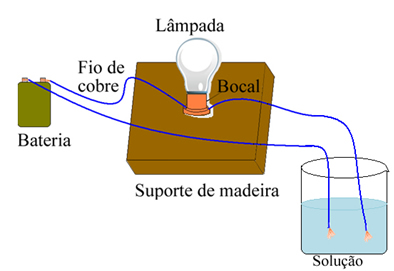
Arrhenius percebeu, por exemplo, que quando ele colocava os eletrodos secos no sal, a lâmpada não acendia, isso também ocorria quando ele os colocava na água pura. Porém, quando ele misturava os dois, dissolvendo o sal na água, a lâmpada acendia, ou seja, a solução formada conduzia corrente elétrica.
No entanto, quando ele colocava o açúcar (C12H22O11) na água, nada acontecia, não havia condução de eletricidade.
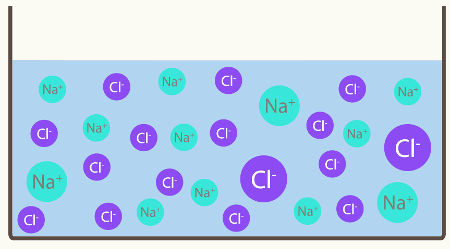
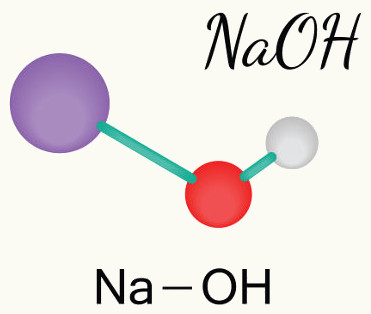
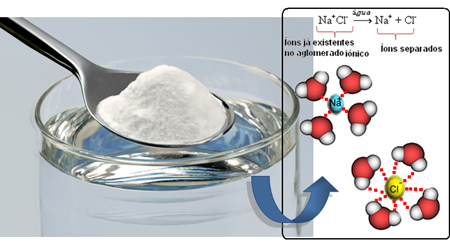
Arrhenius testou várias soluções e percebeu que quando ele colocava compostos iônicos, como o sal de cozinha e a soda cáustica (hidróxido de sódio, NaOH), havia condução de corrente elétrica. Por isso, ele concluiu que a passagem de corrente elétrica se dava porque existiam íons livres na solução, ou seja, os compostos iônicos sofriam dissociação iônica, seus íons eram separados e, por possuírem carga elétrica, conduziam a eletricidade.
Quando ele testou alguns compostos moleculares, como o gás clorídrico (HCl), percebeu que também geravam soluções eletrolíticas que conduziam corrente elétrica. Esse fato se dava porque havia uma ionização* das moléculas do HCl, pois elas reagiam com as moléculas de água, formando íons negativos e positivos:
.jpg)
Assim, nos casos em que há íons livres, temos uma solução eletrolítica, que conduz corrente elétrica.
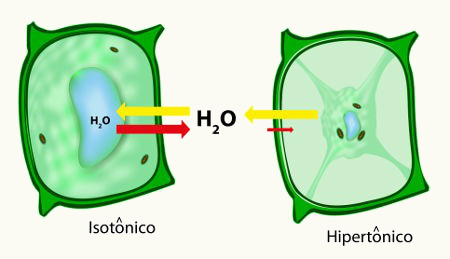
Já no caso do açúcar e de outros compostos moleculares, que mesmo sendo dissolvidos em água não conduzem eletricidade, isso ocorre porque não há liberação de íons no meio, gerando uma solução não eletrolítica. As moléculas de açúcar costumam estar agrupadas em retículos cristalinos, mas quando colocadas em água, essas moléculas se separam, por isso, temos a impressão de que elas “sumiram”, mas, na verdade, as moléculas de C12H22O11 ainda continuam ali e não geram íons.
Baseado nas observações vistas por Arrhenius surgiu também o conceito de ácido, base e sal, que você pode ver no texto Introdução às Funções Inorgânicas.
* Para entender a diferença entre dissociação iônica e ionização, leia o texto abaixo: