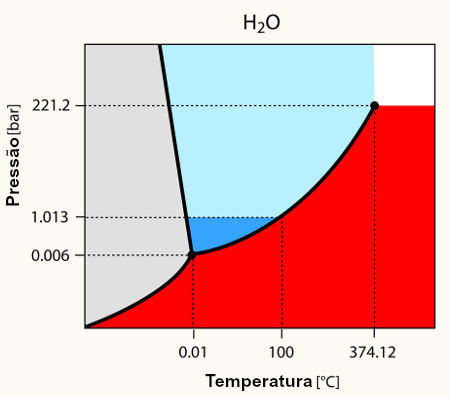
O equilíbrio dinâmico, por sua vez, é o momento em que as fases gasosa e líquida de uma determinada substância permanecem constantes.
Para entender essa questão, pense em uma poça de água. Sabe-se que com o tempo o volume de água dessa poça irá diminuir até secar totalmente; pois, em virtude da agitação das moléculas, elas acabam por adquirir energia cinética e se desprendem da fase líquida. É o que ocorre também com as roupas que secam no varal.
Porém, em uma garrafa fechada, a água em seu interior não tem seu volume alterado. Isso não significa que a água não evapora em recipientes fechados; o que acontece é que, na superfície do líquido, há a passagem constante de moléculas da fase líquida para a gasosa e vice-versa. Ou seja, a mesma quantidade de moléculas que passa para o estado gasoso volta para o líquido; por isso, o volume permanece o mesmo. Essa constância é o equilíbrio dinâmico.
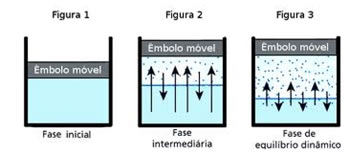
A pressão de vapor de um líquido não depende da quantidade desse líquido. Observe o exemplo abaixo: no primeiro caso temos um volume menor de água, porém a pressão de seu vapor a 25ºC permanece a mesma:
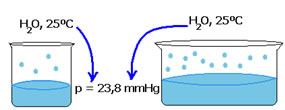
Quando o espaço vazio aumenta, as moléculas têm mais espaço para evaporar. Assim, a pressão de vapor permanece a mesma.
No entanto, existem alguns fatores que interferem na pressão de vapor. Vejamos dois deles:
1. Temperatura – Com o aumento da temperatura, a velocidade de agitação das moléculas também aumenta. Elas ganham mais energia cinética e se desprendem com maior facilidade. Assim, quanto maior a temperatura, maior será a pressão de vapor da substância.
2. Natureza do líquido – Se colocarmos três frascos abertos contendo éter, álcool etílico e água, numa mesma temperatura, veremos com o passar do tempo que o primeiro a evaporar será o éter, posteriormente o álcool e muito depois a água; como pode ser visto no gráfico abaixo.
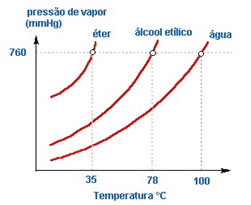
Isso ocorre porque o éter e o álcool são mais voláteis que a água. Ou seja, eles evaporam com maior facilidade porque a interação entre suas moléculas é menos intensa do que as atrações existentes entre as moléculas de água. De tal modo, de uma substância para outra a pressão de vapor varia.

Essa pressão de vapor é medida por um aparelho denominado manômetro e é praticamente desprezível em sólidos. Entretanto, sólidos que sublimam, como o gelo seco e a naftalina, apresentam uma pressão de vapor considerável.