O Ponto de Ebulição (PE) de uma substância é a temperatura em que ela passa do estado líquido para o gasoso (ou estado de vapor).
É importante ressaltar que ebulição é diferente de evaporação, pois apesar de ambas serem a passagem do líquido para o gasoso, estes processos se dão de forma diferente. A evaporação ocorre de forma lenta e somente na superfície da substância. Exemplos de evaporação são: a roupa secando no varal e a evaporação de um rio.
Já a ebulição é quando há um aumento da temperatura e as moléculas passam para o estado gasoso de forma tumultuada e em toda a sua extensão. Exemplo: quando se ferve a água em uma panela.
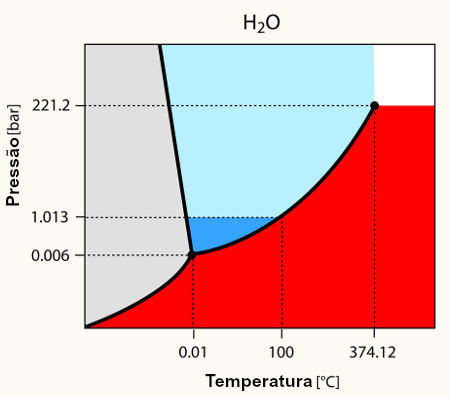
Cada substância tem um valor para o seu PE; o da água é de 100°C ao nível do mar. Se mudarmos a pressão , não sendo ao nível do mar, este valor muda, ou seja, se aumentarmos a pressão, o PE também aumentará e vice-versa.
Vale lembrar também que o valor do PE é igual ao do ponto de condensação ou liquefação. O que determinará se está ocorrendo uma ebulição ou uma condensação será a situação, ou seja, se está aquecendo ou resfriando o sistema.
O Ponto de Fusão (PF) é a temperatura em que certa substância passa do estado sólido para o líquido. Seu valor também é igual ao ponto de solidificação, pois é o caminho inverso, ou seja, a passagem do líquido para o sólido.
No caso da água, ao nível do mar, seu PF é de 0°C. Alguns exemplos de PF e PE estão listados abaixo:

O PE e o PF são considerados propriedades periódicas, isto é, seus valores crescem ou decrescem na medida em que o número atômico dos elementos químicos aumenta e que não se repete em períodos determinados ou regulares.
Assim, na Tabela Periódica, a variação dos PF e PE pode ser representada conforme a figura abaixo:
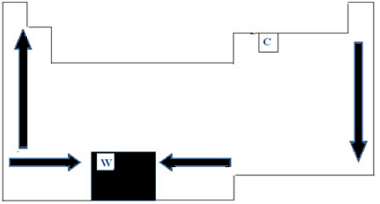
Por possuir o maior PF (3422°C) entre os metais, o tungstênio (W) é utilizado em filamentos de lâmpadas incandescentes. Uma anomalia, que não segue esta representação periódica feita acima, é o carbono. Ele possui PF= 3550°C e PE= 4287°C; isto ocorre porque este elemento tem a propriedade de originar estruturas formadas por um grande número de átomos.
Por Jennifer Fogaça
Graduada em Química.
Videoaula relacionada: