Ligação iônica: é a ligação que ocorre entre íons com a transferência de elétrons. É formada em razão da existência de forças de atração eletrostática entre íons: íons negativos (ânions) e positivos (cátions).
O exemplo mais comum de composto iônico é o Cloreto de Sódio (NaCl), o nosso sal de cozinha. O átomo de sódio (Na) não é estável (apresenta 1 elétron livre na camada de valência), a estabilidade só será atingida se ele perder um elétron, o que dará origem ao cátion Na+. O átomo de cloro (Cl) também não é estável, pelos mesmos motivos que o Na, e atingirá a estabilidade somente se ganhar um elétron, esse átomo dá origem ao íon Cl-. Se os íons já estão formados e eletronicamente estáveis, haverá assim uma interação eletrostática, ou seja, uma ligação iônica que pode ser representada pela equação abaixo.
Na+ + Cl- → NaCl
Ligação metálica: a estrutura atômica dos metais é a Cristalina, que se constitui por cátions do metal envolvidos por elétrons. Os retículos cristalinos presentes nos metais podem ser representados pela figura:

Os retículos cristalinos dos metais são formados por um grupamento de cátions fixos envoltos por elétrons, esses, por sua vez, se encontram deslocalizados, ou seja, não se sentem atraídos por nenhum núcleo.
Ligação covalente: nessa ligação, os átomos são unidos devido ao compartilhar de seus elétrons, surgem então os pares eletrônicos indicados pelo círculo:
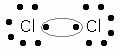
Ligação covalente molecular de dois átomos de Cloro (Cl)
Cada par eletrônico formado pertence simultaneamente aos dois átomos. As moléculas são estruturas eletricamente neutras porque não ocorre nem ganho nem perda de elétrons, apenas o compartilhamento.
Videoaula relacionada: