No cotidiano existem várias situações em que precisamos organizar alguns objetos para facilitar a nossa vida. Por exemplo, quando vamos a um supermercado, os alimentos e outros objetos, como os de higiene e limpeza, estão divididos em seções. Em um mesmo lugar ficam todas as frutas, num lugar próximo ficam as verduras, em outro ficam os legumes. Já numa seção bem distante ficam os materiais de limpeza e assim por diante.
Em casa, podemos organizar os nossos CDs por estilo musical (sertanejo, forró, pagode, funk, jazz, musica popular etc.) e os livros por matéria (Português, Matemática, Filosofia, Química, Física etc.). Outras formas de organização podem ser possíveis nesses casos, como ordem alfabética ou cor do objeto. Enfim, seja qual for o método de classificação utilizado, o objetivo é o mesmo: facilitar a vida de quem irá utilizá-los.
No mesmo modo, os cientistas começaram a observar que os elementos químicos precisavam ser organizados numa ordem que facilitasse o seu estudo. Atualmente, existem cerca de 115 elementos químicos e é preciso organizá-los de um modo que se permita obter mais facilmente informações sobre as suas propriedades e até mesmo prever o seu comportamento.
Dmitri Ivanovich Mendeleev (1834-1907) criou uma tabela periódica que organizava os elementos em ordem crescente de massa atômica. Mas, em 1913, o físico inglês Henry Moseley descobriu experimentalmente os números atômicos (quantidade de prótons) dos elementos e provou que as propriedades que distinguiam cada elemento químico dependiam de seu número atômico respectivo.

RÚSSIA- CIRCA 2009: Selo impresso na Rússia que mostra Dmitri Mendeleev (1834-1907).*
Assim, a Tabela Periódica atual é organizada em ordem crescente de números atômicos.
Os elementos estão organizados indo da esquerda para a direita, aumentando uma unidade no número atômico. Por exemplo, o primeiro elemento que aparece na Tabela Periódica é o hidrogênio, com número atômico igual a 1. O próximo é o hélio, com número atômico igual a 2, o lítio vem em seguida, com número atômico igual a 3 e assim por diante.
Esses elementos também aparecem organizados em linhas verticais que são denominadas de famílias ou grupos dos elementos. Atualmente, as famílias vão de 1 até 18. Os elementos de uma mesma família possuem a mesma quantidade de elétrons na última camada eletrônica e, devido a isso, suas propriedades são semelhantes.
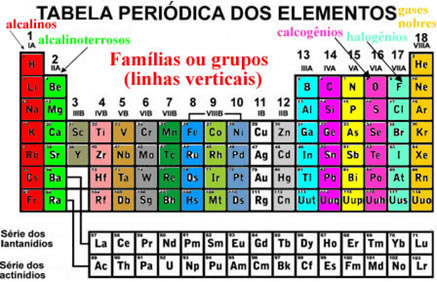
Por exemplo, todos os elementos da família 1 possuem apenas 1 elétron em suas camadas de valência (última camada). O hidrogênio é um elemento que possui propriedades muito diferentes de todos os outros elementos da Tabela Periódica, não se encaixando corretamente em nenhuma família. Porém, ele aparece na família 1 exatamente porque possui só 1 elétron na camada de valência.
Existem algumas famílias da Tabela Periódica que possuem nomes específicos, veja quais são:
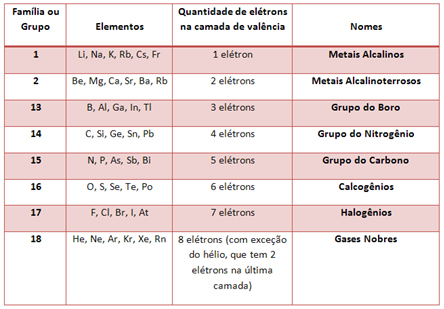
A organização desses elementos também envolve as linhas horizontais, que são os períodos. Os períodos indicam a quantidade de camadas eletrônicas que são preenchidas em cada átomo dos elementos. Por exemplo, todos os elementos do primeiro período possuem apenas uma camada eletrônica, todos do segundo período possuem duas camadas eletrônicas e assim sucessivamente, sendo que os períodos vão de 1 a 7.
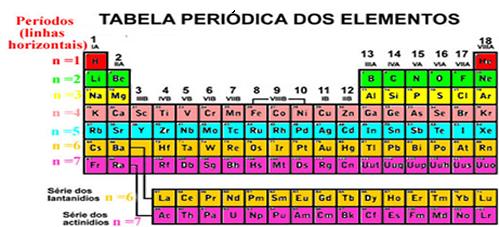
Além disso, os elementos são separados em elementos representativos e em elementos de transição. Antigamente, os elementos representativos eram indicados por serem das famílias que tinham o número acompanhado da letra A (1A, 2A, 3A, 4A, 5A, 6A, 7A e 8A) e os elementos de transição tinham o número acompanhado da letra B (1B, 2B, 3B, 4B, 5B, 6B, 7B e 8B). Porém, esse tipo de nomenclatura não é mais adotado pela IUPAC e agora temos que os elementos representativos estão nas famílias 1, 2, 13 a 18, e os elementos de transição vão das famílias 3 a 12.
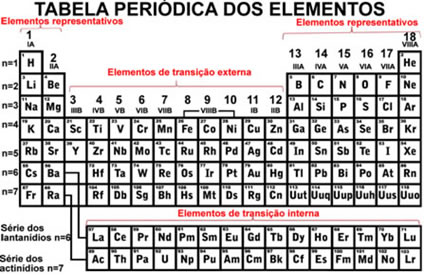
* Créditos da imagem: Olga Popova e Shutterstock.com.
Aproveite para conferir nossas videoaulas sobre o assunto: