Uma molécula polar é aquela que possui diferença de eletronegatividade e se orienta na presença de um campo elétrico externo, já uma molécula apolar não apresenta diferença de eletronegatividade porque os elétrons estão distribuídos sobre todas as moléculas de forma simétrica e, por isso, ela não se orienta na presença de um campo elétrico.
Por exemplo, a água é polar, por isso, se atritarmos um bastão de vidro com lã e o deixarmos eletrizado positivamente, quando o aproximarmos de um filete de água, veremos que ela será atraída pelo bastão. Os polos negativos das moléculas de água são atraídos pelas cargas positivas do bastão.
Para descobrirmos se uma molécula é polar ou apolar precisamos observar dois fatores:
- A diferença de eletronegatividade entre os átomos de cada ligação na molécula;
- Qual é a sua geometria.
As substâncias simples (formadas por átomos de um mesmo elemento químico) são todas apolares, com exceção do ozônio (O3). Alguns exemplos de moléculas assim são: O2, H2, N2, P4, S8.
No entanto, se a substância for composta (formada por mais de um elemento), então teremos que verificar o tipo de geometria da molécula para poder afirmar se ela é polar ou apolar.
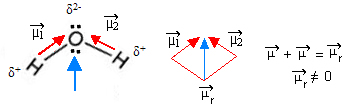
Quando existe diferença de eletronegatividade entre os átomos, surge um dipolo elétrico na molécula, em que o átomo que é mais eletronegativo atrai mais fortemente os elétrons para si e fica com uma carga parcialmente negativa (δ-), enquanto o átomo do outro elemento fica com uma carga parcialmente positiva (δ+).
A soma dos vetores de cada ligação polar é o vetor resultante, que é denominado de Momento de Dipolo ou Momento Dipolar Resultante, sendo simbolizado por ![]() .
.
Esse momento dipolar resultante indica a intensidade das cargas parciais e nos ajuda a determinar a polaridade da molécula. Se o seu valor for igual a zero, isso indica que a molécula é polar. Mas se o valor for diferente de zero, trata-se de uma molécula polar.

O vetor (simbolizado pela seta acima do símbolo) é uma grandeza que é caracterizada pela determinação do seu valor em módulo, pela direção e pelo seu sentido. Vamos fazer uma analogia para você entender como trabalhar com o vetor resultante.
Imagine que uma pessoa esteja puxando um barco que está num lago com uma corda. Considerando que não há outras forças atuando sobre o barco, o barco irá se movimentar no sentido da força aplicada pela pessoa. Esse sentido corresponde ao vetor. Mas se tiverem duas pessoas puxando o barco, a trajetória do barco será determinada pelo vetor resultante entre as forças aplicadas. Por exemplo, se elas estiverem puxando com a mesma intensidade, mas em sentido contrário, um vetor irá anular o outro e o barco permanecerá parado, o vetor resultante será nulo, igual a zero. Mas se eles estiverem puxando conforme a terceira figura abaixo, o sentido em que o barco irá se movimentar será o do vetor resultante:
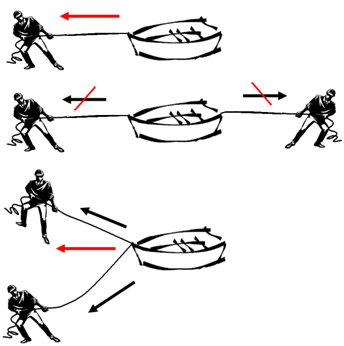
Usaremos o mesmo raciocínio para determinar o momento dipolar resultante das moléculas. Veja alguns exemplos:
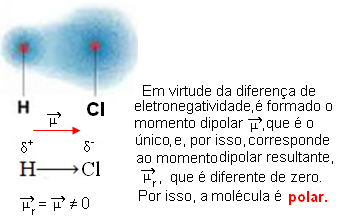
- HCℓ: geometria linear.
O cloro é mais eletronegativo que o hidrogênio, por isso, os elétrons são mais atraídos por ele, criando o seguinte dipolo elétrico:
- CO2: geometria linear.
Os oxigênios são mais eletronegativos que o carbono, atraindo para si os elétrons e criando dois momentos dipolares. O carbono não possui elétrons livres, por isso, os elétrons da ligação que são atraídos por cada oxigênio se arrumam de modo a ficarem o mais longe possível uns dos outros, deixando a molécula com um ângulo de 180º, linear.
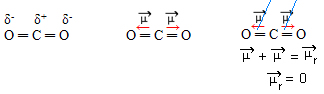
Visto que os vetores dos momentos dipolares são da mesma intensidade e em sentidos opostos, eles se anulam, tendo um momento dipolar resultante igual a zero, por isso, a molécula é apolar.
- H2O: geometria angular.
O oxigênio é o átomo central e é o mais eletronegativo, atraindo os pares de elétrons para si. Sua carga passa a ser negativa (δ2-) e a de cada hidrogênio fica positiva (δ+). Visto que o oxigênio possui 2 pares de elétrons livres, a molécula adquire um ângulo de 104,5º. Desse modo, a soma dos dois momentos dipolares dará um momento dipolar resultante diferente de zero e, devido a isso, a molécula de água é polar.