O mundo ao nosso redor é composto por uma diversidade muito grande de materiais, capazes de realizar fenômenos imprescindíveis para a sustentação da vida.
As propriedades dos materiais, tais como estado físico (sólido, líquido ou gasoso), os pontos de ebulição e fusão, entre outras, devem-se, em grande parte, devido ao tipo de ligação química que seus átomos realizam para a sua formação. Existem três tipos básicos de ligações químicas: a iônica, a covalente e a metálica.
As propriedades principais resultantes de cada uma dessas ligações são:
Substâncias iônicas:
- A atração entre seus íons acaba produzindo aglomerados com formas geométricas bem definidas, denominados retículos cristalinos;
- São sólidas na temperatura ambiente e pressão ambiente (25 ºC e 1atm), porque a força de atração mantém ânions firmemente ligados uns aos outros;
- Apresentam elevados pontos de fusão e ebulição, porque é necessário fornecer uma grande quantidade de energia para romper a atração elétrica existente entre os íons.
- A maioria dessas substâncias são sólidos quebradiços, desestruturam-se quando sofrem algum impacto. Isso ocorre porque ao sofrerem alguma pressão, seus íons de mesma carga se repelem, desestruturando o cristal;
- Conduzem corrente elétrica quando dissolvidas na água e quando fundidas;
- São polares;
O sal (cloreto de sódio – NaCl) exemplifica bem os pontos mencionados acima, pois ele é um composto iônico formado a partir do cátion Na+ e do ânion Cl-.
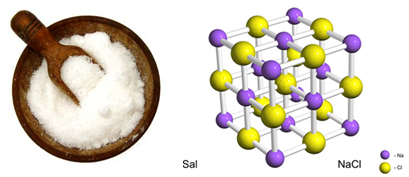
- Possuem elevada dureza, ou seja, possuem grande resistência ao serem riscados por outros materiais.
Substâncias moleculares:
- Em condições ambientes podem ser encontradas nos três estados físicos: gasoso, líquido e sólido. Veja os exemplos:
- Compostos covalentes gasosos: gases oxigênio, nitrogênio e hidrogênio;
- Compostos covalentes líquidos: água
- Compostos covalentes sólidos: sacarose (açúcar), grafite, diamante, enxofre e fósforo.

- Pontos de fusão e ebulição menores que os das substâncias iônicas;
- Podem ser polares ou apolares, depende da diferença de eletronegatividade entre os átomos dos elementos que constituem a ligação;
- Quando puras, não conduzem corrente elétrica.
As ligações covalentes são muito importantes para o organismo humano e para a vida animal e vegetal, pois são por meio delas que se formam as proteínas, aminoácidos, lipídeos, carboidratos e os outros compostos orgânicos.
Substâncias metálicas:
- A maioria dos metais é sólida em condições ambientes. Apenas o mercúrio é encontrado na fase líquida;
- Possuem brilho metálico característico;

- São bons condutores de eletricidade e calor, tanto na fase sólida, quanto na líquida. Por isso, eles são muito usados em fios de alta tensão;
- Possuem densidade elevada, que é resultado das suas estruturas compactas;
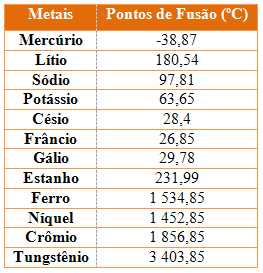
- Possuem pontos de fusão e ebulição elevados. Devido a essa propriedade, eles são usados em locais com grandes aquecimentos, tais como caldeiras, tachos e reatores industriais. O tungstênio (W), por exemplo, é usado em filamentos de lâmpadas incandescentes.

Porém, existem exceções, que são o mercúrio, os metais alcalinos, o índio, o estanho, o bismuto e o gálio. Esse último funde-se apenas com o calor da mão. Veja os pontos de fusão de alguns desses materiais na tabela abaixo:
- São maleáveis (deixam-se reduzir a chapas e lâminas bastante finas) e apresentam ductibilidade (podem ser transformados em fios);

- Apresentam alta tenacidade, suportando pressões elevadas sem sofrer ruptura;
- Elevada resistência à tração, ou seja, são bastante resistentes quando se aplica sobre eles forças de puxar e alongar.
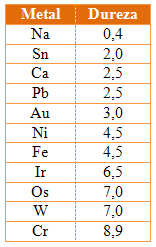
- Em geral, são moles, mas existem exceções, tais como o irídio e o crômio. Veja a tabela a seguir:
As propriedades dos materiais não dependem unicamente do seu tipo de ligação química. Outros fatores como a polaridade, a massa molar e o tipo de forças intermoleculares entre suas moléculas, átomos ou partículas, também são muito importantes.